les dix questions suivantes 11 à 20
|
|
|
|
cinétique chimique -esterification hydrolyse
mélange équimolaire alcool éthylique et acide éthanoique maintenu à 80°C, on dose toutes les 30 minutes l'acide restant.
- Ecrire l'équation bilan; nommer les réactifs et les produits.
- Comment suivre au cours du temps l'évolution de la quantité d'acide restant.
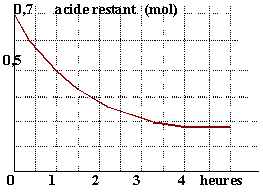
- Déterminer sur le graphe ci contre le temps de demi réaction.
- Comment accéder plus rapidement à l'équilibre?
- Comment déplacer l'équilibre vers la droite , c'est à dire augmenter le rendement en ester?
..

2. faire 8 parts identiques de la solution équimolaire placés dans 8 tubes à essais numérotés, placés dans une étuve à 80°C
toute le 30 minutes sortir un tube, le refroidir (la composition du mélange n'évolue plus)
doser l'acide éthanoique par une solution de soude de concentration connue.
3. temps de demi réaction: date à laquelle la moitié de l'acide initial a disparu
lecture graphe :0,35 en oordonnée donne t=2,5 heures
4. utiliser un catalyseur
travailler à température un peu plus élevée.
5. l'un des réactifs est introduis en excès.
l'un des produits est éliminé au fur et à mesure qu'il se forme
( par distillation fractionnée, le produit le plus volatil s'évapore)
acide base - formes prédominantes
On dissout du chlorure d'ammonium et du méthanoate de sodium dans 1 L d'eau
NH4+ / NH3 pKa=9,2 ;HCOOH / HCOO- pKa=3,8
- Ecrire les équations bilans de ces dissolutions
- Sur un axe gradué de 0 à 14 indiquer les domaines de prédominance de ces 4 espèces.
- Le pH étant égal à 8,5, quelles espèces prédominent.
- Les ions ammonium réagissent ils avec les ions méthanoate ? Si oui, la réaction est elle totale ?
..

la réaction de l'ion ammonium ou de l'ion méthanoate avec l'eau est très limitée
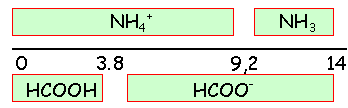
l'ion ammonium et l'ion méthanoate prédomine à pH=8,5.
l'ion ammonium et l'ion méthanoate constituent l'acide et la base les plus faibles. la réaction entre ces ions est très limitée
Kr =10-9,2 / 10-3.8 =10-5,4.
HCOOH / HCOO- pKa=3,8
dosage de l'aspirine
- Quels sont les groupes fonctionnels présents dans la molécule
- On dissout un comprimé dans 100 mL d'eau. 10 mL de cette solution sont dosée par 18 mL de soude de concentration 0,01 mol L-1. Le pH à l'équivalence est 8. L'aspirine est tel un acide fort ?
- On suit l'évolution du pH en fonction du
volume de soude ajouté.
Identifier le couple acide base et donner son pKapH 2,5 3.3 3,5 4 8 10 12 V mL 0 5 9 15 18 20 25 - Ecrire l'équation bilan de la réaction de dosage
- Ecrire l'équation bilan de la réaction de l'aspirine avec l'eau
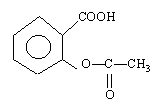 aspirine
ou acide acéthylsalycilique
aspirine
ou acide acéthylsalycilique
..
A la demi équivalence ( 9 mL de soude ajoutée) le pH est égal au pKa du couple. la lecture du tableau donne :pKa=3,5
![]()
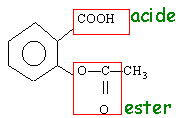
les dérivés des acides carboxyliques
- Dans la molécule ci contre indiquer un centre nucléophile, un carbone asymétrique. Quelle proprièté posséde cette molécule ?
- L'action du chlorure d'éthanoyle sur une amine primaire à chaine carbonnée linéaire donne un composé , noté B de masse molaire 73 g mol-1. A partir de quel acide est obtenu le chlorure d'acyle.
- Donner la formule semi développée du chlorure d'éthanoyle.
- Ecrire l'équation bilan conduisant à B. Identifier le groupe fonctionnel de B
- Quel autre dérivé des acides carboxyliques, agissant sur la même amine , conduirait à B?
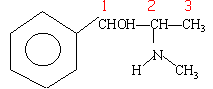
.
Les carbones numérotés 1 et 2 sont tétraédriques et portent 4 substituants différents; ce sont des carbones asymétriques.
Cette molécule est donc chirale possédant deux isomères de configuration ou énantiomères
Le chlorure d'éthanoyle est obtenu à partir de l'acide éthanoique
la masse molaire de R est 73-(2*12+14+16+4) =15 R est CH3.
H3C-COCl + 2 H3C-NH2 donne B + Cl- + H3C-NH3+
L'anhydride éthanoique conduirait au même résultat.
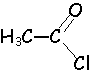
chlorure d'éthanoyle
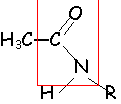
B est un amide
saponification d'un ester, le benzoate d'éthyle(plutot) spécialité
- Quel est le role de la pierre ponce?
- Ecrire l'équation bilan de la réaction. Quelle est son nom.?
- Après calculs des quantités initiales des réactifs, indiquer quel réactif est en défaut. masse molaire du benzoate d'éthyle =150g mol-1.C=12; O=16 ; H=1 ;Na=23
- Identifier le solide obtenu (nom formule).
- Quelle est la quantité théorique ? en déduire le rendement.
..
C6H5COOC2H5 + Na+ +HO- donne C6H5COO- + Na+ + C2H5OH + Na+
benzoate de sodium
la soude est en excès de 0,06 mol
rendement= Qté expérimentale (g)/ Qté théorique (g)
10/ (0,1*144)*100= 70%
bobine longue ou solénoide
Un solénoide de longueur 50 cm compte 500 spires. On place une aiguille aimantée , mobile autour d'un axe verticale, au centre de la bobine. Cette aiguille est perpendiculaire à l'axe de la bobine lorsque l'intensité du courant est nulle.
- Quelle est la direction prise par cette aiguille ?
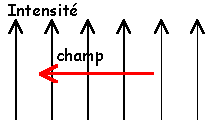
- La bobine est maintenant parcourue par un courant continu d'intensité I= 20 mA. Faire un schéma en indiquant le sens du courant et les caractéristiques du champ magnétique.
- De quel angle la petite aiguille va t-elle tourner ? schéma et détails du calculs
composante horizontale du champ terrestre 2 10-5 T. et m0=4p 10-7 SI
.
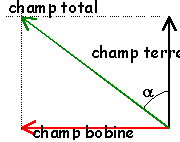
Le champ magnétique est uniforme à l'intérieur du solénoide (sauf au voisinage des extrémités); Ce champ est proportionnel à l'intensité du courant I ; Ce champ sens de sens si le courant change de sens.
B=4p 10-7 n I
n nombre de spires par mètre soit 1000
I =0,04 A alors B=2,5 10-5 T
l'aiguille aimantée s'oriente suivant le champ total, somme vectorielle des deux champs et tourne d'un angle a tel que tan (a)=2,5 / 2 = 1,25
a=51,3 °
.
un avion catapulté...
Les avions de combat sont catapultés sur une distance de 25 m, lors du décollage sur un porte avion. La vitesse de l'avion , à la fin du lancement est 180 km h-1.L'accélération est supposée constante au cours du catapultage.
- Etablir la relation ente distance, vitesse et accélération.
- Quelle est la valeur de l'accéleration?
- Ecrire l'équation horaire du mouvement
- Quelle est la durée du catapultage?
.
vitesse finale 180 /3,6 =50 ms-1.
accélération =50*50 /50=50 ms-2.
25=0,5*50*t2 d'où t=1 s
V2 finale =2 accélération*distance
x=0,5 *a*t2
un pendule dans un véhicule en mouvement
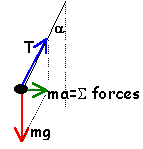
Un pendule est constitué par un fil de longueur l et de masse négligeable. A une extrémitéon fixe une bille de masse m; l'autre extrémité est accrochée au plafond du véhicule.
- L'auto démarre avec une accélération constante : exprimer l'angle d'inclinaison du fil en fonction de l'accélération.
- Exprimer la tension du fil en fonction des données.
- l'auto est animé d'un mouvement rectiligne uniforme: mêmes questions
..
tension T=mg / cos(a)

mvt uniforme
démarrage
le circuit LC - oscillations libres amorties ou non
Un condensateur chargé de capacité C=100 nF est mis en série avec une bobine d'inductance L=1 mH et de résistance négligeable.
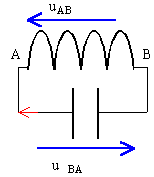
- Donner les expressions des tensions aux bornes du condensateur et de la bobine. Faire des schémas.
- établir l'équation différentielle qui relie la charge q, la capacité et l'inductance
- Un oscilloscope est branché aux bornes du condensateur. Donner l'allure de la courbe observée.Quelle est sa fréquence?
- Comment évolue la courbe précédente si la résistance du circuit n'est plus négligeable.
.
l'équation différentielle s'obtient
en écrivant que uAB + uBA=0
on observe une sinusoïde de fréquence 15924 Hz;
les oscillations sont libres, périodiques si la résistance du circuit est nulle; elles sont libres mais d'autant plus amorties que la résistance est grande.
![]()
![]()
![]()
circuit RLC série - oscillations forcées
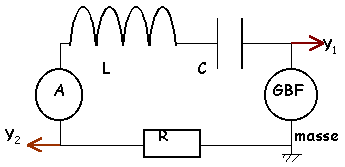
Un circuit RLC série est alimenté par un générateur délivrant un signal sinusoïdal de fréquence variable et de tension éfficace constante égale à 4 V. Un ampèremètre mesure l'intensité éfficace I. Un oscilloscope visualise la tension aux bornes du circuit RLC et d'autre part l'image de l'intensité.
- Proposer le schéma du montage en indiquant les branchements de l'oscilloscope
- Pour quelle fréquence du générateur obtient-on la résonance?.Cette fréquence dépend-elle de la résistance?
- Que deviennent l 'intensité, l'impédance du dipole RLC, et la tension aux bornes du condensateur à la résonance.
..
Lorsque la fréquence du générateur est égale à la fréquence propre du dipole RLC, on observe le phénomène de résonance d'intensité. Cette fréquence est indépendante de R; elle ne dépend que de L et C.
L'intensité passe par une valeur maxi;
l'impédance du circuit passe par une valeur minimale égale à la résistance du circuit
la tension aux bornes du condensateur augmente ( surtension égale à la tension aux bornes du GBF multipliée par le facteur de qualité); cette surtension est d'autant plus grande que la résonance est aigue.
retour - menu